El descubrimiento de la estructura del ADN en forma de doble hélice fue uno de los más importantes de la historia de la genética.
Miriam Barchilón, 29/10/2019
El descubrimiento del ácido desoxiribonucleico (ADN) cambió para siempre la comprensión de la genética, el estudio sobre cómo se transmite la herencia física y fisiológica de generación en generación.
La molécula de ADN se identificó por 1ª vez en la IIª mitad del siglo XIX. Un siglo después, a mitad del s.XX, empezó la edad dorada de los descubrimientos en genética, cuando se definió la estructura y funcionamiento del código genético.
Hoy en día, los científicos se centran en investigar cómo editar el ADN para corregir errores y curar enfermedades de origen genético.
Los inicios de la genética en el s. XIX
El ADN fue aislado por 1ª vez en 1869 por el biólogo suizo Johan Friedrich Miescher. Mientras estudiaba la composición química de los glóbulos blancos, observó que dentro de las células había una sustancia aislada rica en fosfatos, sin azufre y resistente a las proteasas, algo que no se correspondía a la estructura típica de los lípidos o proteínas.
Miescher bautizó esa nueva molécula como nucleína, ya que se encontraba en el núcleo de todas las células estudiadas.
Johan Friedrich Miescher, realizó investigaciones y descubrimientos preliminares sobre el ADN aislando moléculas ricas en fosfato a partir de núcleos de glóbulos blancos.
Posteriormente fueron denominadas “Acidos Nucleicos”.
Entre 1885 y 1901, la composición química del ADN empezó a definirse. En 1889 Richard Altmann, patólogo alemán que había sido discípulo de Miescher, redefinió esta sustancia con el término “ácido nucleico”.
Por su parte, el médico alemán Albert Kossel descubrió la existencia de hidratos de carbono y de unos compuestos o bases nitrogenadas a las que llamó “adenina”, “guanina”, “citosina” y “timina” dentro de la molécula de ADN.
Entre 1885 y 1901, la composición química del ADN empezó a definirse. En 1889 Richard Altmann, patólogo alemán que había sido discípulo de Miescher, redefinió esta sustancia con el término “ácido nucleico”.
Por su parte, el médico alemán Albert Kossel descubrió la existencia de hidratos de carbono y de unos compuestos o bases nitrogenadas a las que llamó “adenina”, “guanina”, “citosina” y “timina” dentro de la molécula de ADN.
Este descubrimiento le valió el Premio Nobel de Medicina en 1910.
La revolución del ADN
El siglo XX empezó con grandes avances en la investigación del ADN. Durante la década de 1920, el bioquímico ruso-estadounidense Phoebus Levene determinó la existencia del ARN, otro ácido nucleico necesario para la transmisión de información genética.
Levene también detectó la presencia de grupo fosfato y de un tipo de azúcar llamado ribosa, 2 componentes imprescindibles en la formación del ADN. Más tarde, el bioquímico descubrió que el grupo fosfato, el azúcar y las bases nitrogenadas se unían para formar nucleótidos.
ESTRUCTURA DEL ADN. Cada nucleótido está formado por 3 unidades: una molécula de azúcar llamada desoxirribosa, un grupo fosfato y uno de 4 posibles compuestos nitrogenados llamados bases: Adenina (A), Guanina (G), Timina (T) y Citosina(C).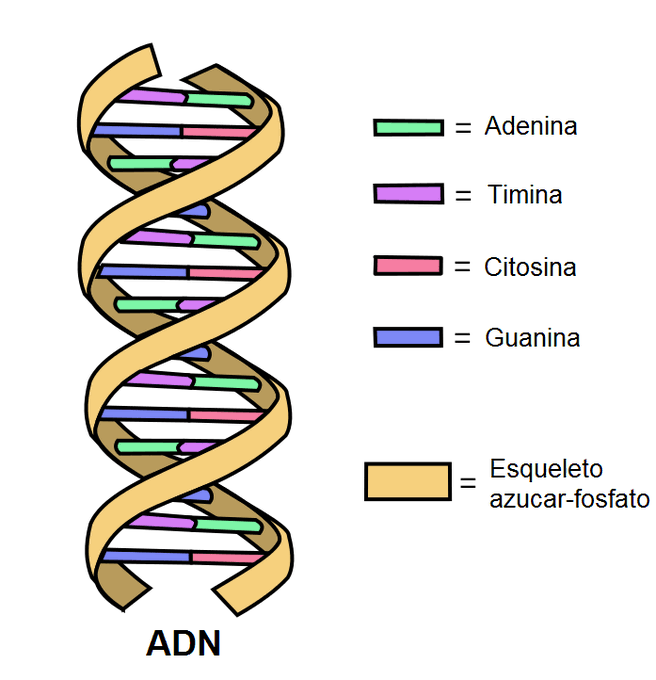
Durante los años siguientes se llevaron a cabo varios experimentos que concluyeron que el ADN era la molécula responsable de la herencia: los estudios del microbiólogo Frederick Griffith, los hallazgos de Oswald Avery en 1944 y los experimentos de Alfred Hershey y Martha Chase en 1952.
El avance más importante en este campo se produjo en 1953, cuando el físico Francis Crick y el biólogo James Watson demostraron la estructura de doble hélice del ADN. Recibieron el Premio Nobel de Medicina en 1962 junto al físico Maurice Wilkins.
Sin embargo, su hallazgo no hubiera sido posible sin la labor de la química Rosalind Franklin, responsable de la famosa Fotografía 51 que revelaba la forma helicoidal de la molécula de ADN. Wilkins, que compartía laboratorio con ella, tomó la fotografía sin su permiso y gracias a eso hicieron el gran descubrimiento.
Tras el descubrimiento de la estructura del ADN, atribuido a Maurice Wilkins, Francis Crick y James Watson, hay un episodio tan fascinante como triste: La omisión del papel clave de Raymond Gosling y Rosalind
Franklin.
Una vez descubierta la forma y composición del ADN, los estudios más recientes se centran en su funcionamiento: ver qué reacciones químicas se producen dentro de la célula para intentar reproducirlas en el laboratorio.
De esta forma, las técnicas de edición genética tienen como objetivo modificar el código genético de algunas células cuyo ADN es incorrecto o está dañado, lo que puede provocar trastornos y enfermedades.
La revolución del ADN
El siglo XX empezó con grandes avances en la investigación del ADN. Durante la década de 1920, el bioquímico ruso-estadounidense Phoebus Levene determinó la existencia del ARN, otro ácido nucleico necesario para la transmisión de información genética.
Levene también detectó la presencia de grupo fosfato y de un tipo de azúcar llamado ribosa, 2 componentes imprescindibles en la formación del ADN. Más tarde, el bioquímico descubrió que el grupo fosfato, el azúcar y las bases nitrogenadas se unían para formar nucleótidos.
ESTRUCTURA DEL ADN. Cada nucleótido está formado por 3 unidades: una molécula de azúcar llamada desoxirribosa, un grupo fosfato y uno de 4 posibles compuestos nitrogenados llamados bases: Adenina (A), Guanina (G), Timina (T) y Citosina(C).

Durante los años siguientes se llevaron a cabo varios experimentos que concluyeron que el ADN era la molécula responsable de la herencia: los estudios del microbiólogo Frederick Griffith, los hallazgos de Oswald Avery en 1944 y los experimentos de Alfred Hershey y Martha Chase en 1952.
El avance más importante en este campo se produjo en 1953, cuando el físico Francis Crick y el biólogo James Watson demostraron la estructura de doble hélice del ADN. Recibieron el Premio Nobel de Medicina en 1962 junto al físico Maurice Wilkins.
Sin embargo, su hallazgo no hubiera sido posible sin la labor de la química Rosalind Franklin, responsable de la famosa Fotografía 51 que revelaba la forma helicoidal de la molécula de ADN. Wilkins, que compartía laboratorio con ella, tomó la fotografía sin su permiso y gracias a eso hicieron el gran descubrimiento.
Tras el descubrimiento de la estructura del ADN, atribuido a Maurice Wilkins, Francis Crick y James Watson, hay un episodio tan fascinante como triste: La omisión del papel clave de Raymond Gosling y Rosalind
Franklin.
Una vez descubierta la forma y composición del ADN, los estudios más recientes se centran en su funcionamiento: ver qué reacciones químicas se producen dentro de la célula para intentar reproducirlas en el laboratorio.
De esta forma, las técnicas de edición genética tienen como objetivo modificar el código genético de algunas células cuyo ADN es incorrecto o está dañado, lo que puede provocar trastornos y enfermedades.


